- Tóm tắt
- 19 Tháng Ba 2024
- Giới thiệu
- Các loại dữ liệu và bộ dữ liệu để phân tích khối u não
- Những tiến bộ trong tiền xử lý tăng cường AI để phân tích khối u não chính xác
- AI trong chẩn đoán khối u não
- X quang được hỗ trợ bởi AI và các phương pháp chẩn đoán dựa trên mô học
- AI trong tiên lượng khối u não
- AI trong quản lý điều trị khối u não
- Phân tích tích hợp đa phương thức và đa quy mô
- Những thách thức và hạn chế của AI trong chẩn đoán, tiên lượng và điều trị khối u não
- Ý nghĩa đạo đức, pháp lý và xã hội của AI trong quản lý khối u não
- Sự thảo luận
- Một tầm nhìn cho tương lai: một loạt các phương pháp tiếp cận
- Kết luận
Trí tuệ nhân tạo trong ung thư thần kinh: những tiến bộ và thách thức trong chẩn đoán, tiên lượng và điều trị chính xác khối u não
Tóm tắt
Đánh giá này đi sâu vào những tiến bộ gần đây nhất trong việc áp dụng trí tuệ nhân tạo (AI) trong ung thư thần kinh, đặc biệt nhấn mạnh công việc về u thần kinh đệm, một loại khối u não đại diện cho một vấn đề sức khỏe toàn cầu quan trọng. AI đã mang lại những đổi mới mang tính biến đổi để quản lý khối u não, sử dụng các công cụ hình ảnh, mô bệnh học và bộ gen để phát hiện, phân loại, dự đoán kết quả và lập kế hoạch điều trị hiệu quả. Đánh giá ảnh hưởng của nó trên tất cả các khía cạnh của quản lý khối u não ác tính – chẩn đoán, tiên lượng và điều trị – các mô hình AI vượt trội hơn các đánh giá của con người về độ chính xác và độ đặc hiệu. Khả năng phân biệt các khía cạnh phân tử từ hình ảnh có thể làm giảm sự phụ thuộc vào chẩn đoán xâm lấn và có thể đẩy nhanh thời gian chẩn đoán phân tử. Bài đánh giá bao gồm các kỹ thuật AI, từ học máy cổ điển đến học sâu, làm nổi bật các ứng dụng và thách thức hiện tại. Các hướng đi đầy hứa hẹn cho nghiên cứu trong tương lai bao gồm tích hợp dữ liệu đa phương thức, AI tạo ra, các mô hình ngôn ngữ y tế lớn, mô tả và mô tả khối u chính xác, và giải quyết sự chênh lệch về chủng tộc và giới tính. Các chiến lược điều trị cá nhân hóa thích ứng cũng được nhấn mạnh để tối ưu hóa kết quả lâm sàng. Ý nghĩa đạo đức, pháp lý và xã hội được thảo luận, ủng hộ tính minh bạch và công bằng trong tích hợp AI cho ung thư thần kinh và cung cấp sự hiểu biết toàn diện về tác động biến đổi của nó đối với chăm sóc bệnh nhân.
19 Tháng Ba 2024
Giới thiệu
Các khối u hệ thần kinh trung ương (CNS), dù là nguyên phát hay thứ phát, đều có tác động đáng kể đến sức khỏe toàn cầu, chiếm hơn 250.000 trường hợp được báo cáo hàng năm, đánh dấu chúng là mối quan tâm toàn cầu đáng kể1,2. Năm 2022, ước tính có khoảng 26.670 khối u ác tính và 66.806 khối u thần kinh trung ương không ác tính được chẩn đoán trong dân số Hoa Kỳ3. Đáng chú ý, u nguyên bào thần kinh đệm, một loại khối u não phát triển nhanh, hung dữ và ác tính, nổi lên như một đóng góp chính cho tỷ lệ mắc bệnh và tử vong ở các khối u não trưởng thành, thể hiện tỷ lệ sống sót sau 5 năm đáng lo ngại 6,9% và góp phần gây ra 10.000 ca tử vong hàng năm ở Mỹ4,5. Những con số này làm nổi bật những thiếu sót hiện tại trong điều trị khối u não.
Mặc dù có nhiều thử nghiệm lâm sàng và nhiều thập kỷ nghiên cứu, các khối u não không thể chữa khỏi với tiên lượng nghiệt ngã vẫn tồn tại, chẳng hạn như u thần kinh đệm đường giữa lan tỏa (DMG) thấy ở trẻ em và u nguyên bào thần kinh đệm ở người lớn6. Sự khẩn cấp này nhấn mạnh sự cần thiết của một phương pháp điều trị cá nhân hóa, có thể mang lại khả năng chữa khỏi cao nhất trong khi giảm thiểu độc tính tiềm ẩn cho bệnh nhân. Tuy nhiên, việc phát triển các chiến lược cá nhân hóa phải đối mặt với những trở ngại do khó khăn trong việc khái quát hóa các phương pháp tiếp cận có nguồn gốc từ dữ liệu có nguồn gốc từ một tổ chức đơn lẻ hoặc một tập đoàn hạn chế của các tổ chức và hạn chế quyền truy cập vào các công nghệ tiên tiến và thử nghiệm lâm sàng, chủ yếu tập trung ở các trung tâm chuyên ngành7. Điều này trở thành một mối quan tâm quan trọng, đặc biệt là khi suy ngẫm về các phân nhánh đạo đức liên quan đến việc phát triển các phương pháp tiếp cận dựa trên dữ liệu thiếu đại diện trên các nhân khẩu học đa dạng. Đáng báo động, những người bị u nguyên bào thần kinh đệm từ các nền kinh tế xã hội thấp hơn ít có khả năng trải qua xét nghiệm O6-Methylguanine-DNA-methyltransferase (MGMT)8. Sự vắng mặt của xét nghiệm MGMT có thể làm sai lệch dự đoán và góp phần chẩn đoán giai đoạn cuối với các khối u lớn hơn và khó khăn hơn. Hơn nữa, nhân khẩu học này ít được cung cấp với sự kết hợp của các phương thức điều trị đa dạng, dẫn đến tỷ lệ sống sót thấp hơn9.
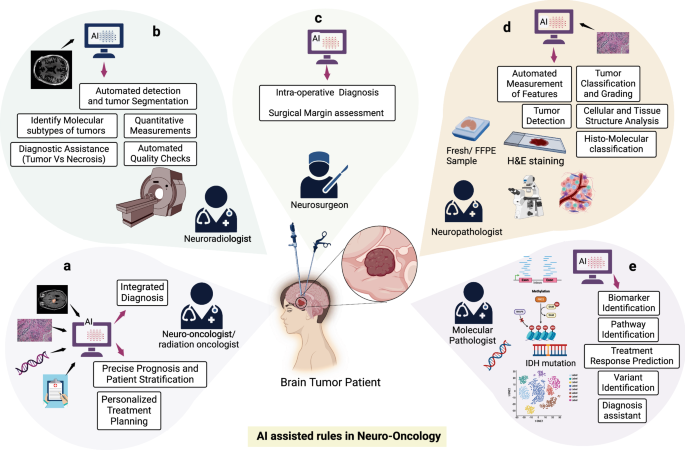
Đối với một bệnh nhân bị nghi ngờ chứa u não, đánh giá thường bắt đầu bằng khám sức khỏe và hình ảnh thần kinh, sau đó là sinh thiết hoặc cắt bỏ khối u trong trường hợp khả thi và phân tích mô học và phân tử tiếp theo của mô chiết xuất được thực hiện thông qua bệnh lý. Nếu thấy cần thiết, cũng có thể thực hiện đánh giá dấu ấn sinh học trong huyết thanh hoặc dịch não tủy (CSF)10. Sau những đánh giá này, nhóm lâm sàng phải quyết định liệu pháp tối ưu, xem xét tiêu chuẩn chăm sóc, các thử nghiệm lâm sàng đang diễn ra, bệnh đi kèm của bệnh nhân và nguy cơ độc tính. Đáp ứng điều trị được theo dõi theo chiều dọc thông qua MRI nối tiếp và, đôi khi, các dấu ấn sinh học máu hoặc dịch não tủy khác11. Các quyết định liên quan đến điều trị khối u não thường liên quan đến các cuộc họp đa ngành giữa các bác sĩ ung thư thần kinh, bác sĩ phẫu thuật thần kinh, bác sĩ X quang thần kinh, nhà nghiên cứu bệnh học phân tử và nhà thần kinh học, nhấn mạnh sự phức tạp của các quyết định này12 (Hình. 1).
AI tăng cường khả năng của các bác sĩ ung thư thần kinh / bác sĩ ung thư bức xạ bằng cách cho phép chẩn đoán tích hợp, cung cấp những hiểu biết sâu sắc hơn về bệnh, tạo điều kiện tiên lượng chính xác bằng cách dự đoán kết quả và hỗ trợ phân tầng bệnh nhân để điều chỉnh kế hoạch điều trị theo nhu cầu cá nhân. b AI hỗ trợ các bác sĩ X quang thần kinh bằng cách tận dụng hình ảnh MRI để phát hiện tự động và phân đoạn khối u, xác định các phân nhóm phân tử của khối u, cung cấp các phép đo định lượng và cung cấp hỗ trợ chẩn đoán để phân biệt khối u với các vùng hoại tử, đồng thời đảm bảo kiểm tra chất lượng tự động. c AI hỗ trợ các bác sĩ phẫu thuật thần kinh trong quá trình phẫu thuật, góp phần đánh giá biên độ phẫu thuật và cung cấp thông tin và hướng dẫn chẩn đoán theo thời gian thực, nâng cao độ chính xác của phẫu thuật và kết quả của bệnh nhân. d AI hỗ trợ các nhà thần kinh học trong việc phân tích các mẫu mới / FFPE, cung cấp phép đo tự động các tính năng, hỗ trợ phân loại và phân loại khối u, cải thiện phát hiện khối u và phân tích toàn diện cấu trúc tế bào và mô thông qua phân loại mô phân tử. e Xử lý dữ liệu đột biến, thông tin tế bào đơn, mẫu methyl hóa, trình tự RNA, v.v., AI trao quyền cho các nhà nghiên cứu bệnh học phân tử bằng cách hỗ trợ xác định dấu ấn sinh học, xác định con đường, dự đoán đáp ứng điều trị, xác định biến thể và đóng vai trò trợ lý chẩn đoán, hợp lý hóa quy trình phân tích phân tử phức tạp (Được tạo bằng BioRender.com).
Tuy nhiên, các bước này trong quản lý bệnh có nhiều thách thức và sai sót có thể dẫn đến tỷ lệ mắc bệnh và tử vong của bệnh nhân13. Những thách thức bao gồm nhu cầu chẩn đoán và dàn dựng bệnh chính xác để hướng dẫn các quyết định lâm sàng, theo dõi liên tục tiến triển bệnh sau điều trị, có thể phức tạp bởi các tín hiệu từ mô thần kinh lân cận và ý nghĩa ngày càng tăng của việc xác định các mẫu kiểu gen14. Những mẫu kiểu gen này có tác động đáng kể đến hành vi của khối u và kết quả lâm sàng15. Cuối cùng, những thách thức trong việc quản lý khối u não phát sinh từ nhiều yếu tố khác nhau, bao gồm sự phức tạp của não, khả năng tiếp cận hạn chế đối với các thủ tục hình ảnh và sinh thiết chính xác, tính không đồng nhất vốn có của sinh học khối u, tỷ lệ tiến triển thay đổi, sự thay đổi cá nhân trong tính nhạy cảm với điều trị và thiếu tương đối các dấu ấn sinh học đáng tin cậy dự đoán tiên lượng1,16,17. Sự nhạy cảm của mô thần kinh với các phương thức điều trị tiêu chuẩn, bao gồm phẫu thuật, xạ trị và hóa trị, làm phức tạp thêm việc chăm sóc của họ18.
Trí tuệ nhân tạo (AI) hứa hẹn là một công cụ biến đổi trong ung thư thần kinh, hiện đang giải quyết các thách thức trong các giai đoạn quản lý lâm sàng khác nhau. Trong quản lý khối u não, AI thể hiện tiềm năng của nó thông qua chẩn đoán, tiên lượng và lập kế hoạch điều trị bằng cách tăng tốc và tăng cường hình ảnh MRI19, phát hiện bất thường, tối ưu hóa quy trình làm việc, cung cấp các phép đo chính xác, phân tích dữ liệu hình ảnh y tế rộng rãi và xác định các mẫu không dễ nhận ra đối với người quan sát20. Nó đã nâng cao đáng kể lĩnh vực này bằng cách cung cấp phân tích hình ảnh chi tiết để chẩn đoán, phân loại khối u, xác định tiên lượng và đánh giá đáp ứng điều trị. Nó cũng tạo điều kiện cho việc lập kế hoạch điều trị phẫu thuật và không phẫu thuật21, đẩy nhanh quá trình khám phá thuốc22và tạo điều kiện theo dõi tái phát. Các công cụ AI có thể được tích hợp vào các thử nghiệm lâm sàng, nhằm cải thiện kết quả của bệnh nhân và có thể cung cấp con đường hướng tới liệu pháp cá nhân hóa15,23. Trong hình ảnh thần kinh lâm sàng, AI đóng một vai trò quan trọng trong các nhiệm vụ như xác định ranh giới và loại khối u, tinh chỉnh kế hoạch tiền trị liệu và đánh giá phản ứng sau điều trị24. Khả năng AI xử lý các bộ dữ liệu mở rộng cung cấp một cách tiếp cận biến đổi đối với y học chính xác, có khả năng giải quyết các điểm đau thường gặp ở tất cả các bước của trải nghiệm chăm sóc bệnh nhân25,26,27 (Hình. 1). Ngoài ra, nó hứa hẹn trong việc cải thiện sự chênh lệch chăm sóc sức khỏe toàn cầu bằng cách cung cấp quyền truy cập dân chủ vào các chiến lược chẩn đoán, tiên lượng và điều trị28,29.
Gần đây, đã có sự khám phá ngày càng tăng về việc tích hợp các công cụ AI vào quy trình làm việc X quang và bệnh lý, cho thấy những tiến bộ tiềm năng trong ung thư thần kinh30,31. Trong phân tích khối u não, AI đóng vai trò là một khuôn khổ toàn diện bao gồm các kỹ thuật học máy (ML) và học sâu (DL), thị giác máy tính (CV) và tích hợp chúng vào Sinh học tính toán. Các thuật toán ML trong AI góp phần nhận dạng mẫu trong dữ liệu hình ảnh và gen, trong khi DL, một tập hợp con của ML, vượt trội trong việc trích xuất tính năng phức tạp. Thị giác máy tính, cho dù thông qua các kỹ thuật xử lý hình ảnh cổ điển hay phương pháp DL tiên tiến, diễn giải dữ liệu hình ảnh để phân tích hình ảnh y tế chính xác. Sinh học tính toán tận dụng AI, ML và DL để phân tích các bộ dữ liệu sinh học mở rộng, giúp hiểu các khía cạnh di truyền và phân tử của khối u não (Bảng bổ sung 1). Sức mạnh tổng hợp giữa các kỹ thuật này giúp tăng cường độ sâu và độ chính xác của đặc tính khối u não, ảnh hưởng đến chẩn đoán, tiên lượng và lập kế hoạch điều trị.
Khi tiến hành đánh giá này, một tìm kiếm tài liệu toàn diện đã được thực hiện trên một số cơ sở dữ liệu điện tử. Việc tìm kiếm tập trung vào các bài báo được xuất bản gần đây, tập trung vào các nghiên cứu liên quan đến các ứng dụng AI trong chẩn đoán, tiên lượng và điều trị chính xác khối u não. Chiến lược tìm kiếm của chúng tôi ưu tiên các bài viết được đánh giá ngang hàng, đánh giá có hệ thống, phân tích tổng hợp và nghiên cứu mang tính bước ngoặt trong lĩnh vực này. Đánh giá tường thuật này cung cấp một sự hiểu biết toàn diện về vai trò quan trọng của AI trong việc quản lý các khối u não ác tính nguyên phát, tập trung vào u thần kinh đệm. Nó khám phá các ứng dụng AI trong chẩn đoán khối u não, tiên lượng, lập kế hoạch điều trị và phân tích dự đoán. Giải quyết bản chất nhiều mặt của AI trong ung thư thần kinh, chúng tôi thảo luận về các dấu ấn sinh học, ý nghĩa đạo đức, phương pháp sáng tạo và thách thức, bao gồm cả những cân nhắc về sự khác biệt cụ thể về chủng tộc và giới tính trong các ứng dụng AI và nỗ lực giải quyết sự chênh lệch trong giới hạn công việc hiện tại. Điều làm cho đánh giá của chúng tôi khác biệt là tập trung rõ ràng vào việc tích hợp AI trong X quang, bệnh lý và bộ gen để phân tích khối u não toàn diện. Không giống như các bài báo trước, đánh giá của chúng tôi nhấn mạnh sự hội tụ của các ứng dụng AI trên X quang, bệnh lý và bộ gen, cung cấp một cách tiếp cận toàn diện để chẩn đoán, tiên lượng và lập kế hoạch điều trị khối u não. Mặc dù nhiều đánh giá trước đây đã thảo luận rộng rãi về AI trong ung thư thần kinh, nhưng chúng thường thiếu sự nhấn mạnh cụ thể về sự tích hợp hiệp đồng của AI trên các lĩnh vực quan trọng này. Tập trung vào việc lập kế hoạch chẩn đoán, tiên lượng và điều trị trong lĩnh vực hình ảnh, bài báo của chúng tôi không chỉ khám phá những tiến bộ mới nhất trong AI phù hợp với bệnh lý, X quang và bộ gen mà còn giải quyết những khoảng trống do các đánh giá trước đó để lại trong việc hiểu đầy đủ vai trò liên kết của các ngành này trong quản lý khối u não. Cách tiếp cận tập trung này đóng góp một quan điểm độc đáo, nêu chi tiết vai trò biến đổi của AI trong việc tinh chỉnh các chẩn đoán, tiên lượng và lập kế hoạch điều trị dựa trên hình ảnh, vốn không được bao phủ kỹ lưỡng bởi các đánh giá rộng hơn, ít chuyên môn hơn trong lĩnh vực này.
Các loại dữ liệu và bộ dữ liệu để phân tích khối u não
Phân tích khối u não dựa trên một loạt các loại dữ liệu được sử dụng hiệu quả bởi các thuật toán AI để tiết lộ các đặc điểm quan trọng. Các danh mục dữ liệu chính bao gồm dữ liệu hình ảnh, dữ liệu gen và dữ liệu lâm sàng. Các kỹ thuật hình ảnh y tế, chẳng hạn như MRI và CT, cung cấp cơ hội để trích xuất các đặc điểm thị giác phức tạp về kích thước, vị trí, hình thái và kết cấu khối u. Tiêu chuẩn hiện tại cho hình ảnh khối u não liên quan đến MRI đa tham số, bao gồm các trình tự như trọng số T1 trước và sau tương phản, trọng số T2, phục hồi đảo ngược giảm chất lỏng (FLAIR), trọng số khuếch tán (DWI) và hình ảnh trọng số nhạy cảm (SWI) như các trình tự thường thu được. Các trung tâm ung thư thần kinh khối lượng lớn thường kết hợp các kỹ thuật bổ sung như quang phổ MR và hình ảnh tưới máu11,32. Ngoài hình ảnh tiêu chuẩn, radiomics trích xuất các đặc điểm định lượng, trong khi dữ liệu mô bệnh học, có nguồn gốc từ sinh thiết hoặc phẫu thuật cắt bỏ, bao gồm hình thái tế bào khối u và kiến trúc mô. Dữ liệu gen, bắt nguồn từ trình tự DNA và RNA, phân tích phiên mã và phân tích methyl hóa, hỗ trợ phân loại các phân nhóm và dự đoán sự xâm lấn của khối u33. Hơn nữa, các dấu ấn sinh học phân tử nổi bật đóng một vai trò quan trọng trong việc phân biệt giữa các phân nhóm khối u não1,9,34. Chúng bao gồm đột biến IDH đối với u tế bào hình sao và u oligodendrogliomas, đột biến chất kích thích TERT đối với u nguyên bào thần kinh đệm, khuếch đại EGFR đối với u nguyên bào thần kinh đệm, tăng nhiễm sắc thể 7 và mất nhiễm sắc thể 10 đối với u nguyên bào thần kinh đệm, đột biến ATRX đối với u tế bào hình sao, methyl hóa chất kích thích MGMT đối với u nguyên bào thần kinh đệm, đồng xóa nhiễm sắc thể 1p và 19q đối với u oligodendroglia và các phân nhóm phân tử riêng biệt cho u nguyên bào tủy (MB)9 (Xem Bảng 2 và 3). Cuối cùng, Dữ liệu lâm sàng, bao gồm lịch sử bệnh nhân, hồ sơ y tế và đáp ứng điều trị, góp phần vào hồ sơ chẩn đoán toàn diện, với dữ liệu kết quả đóng vai trò là tài liệu tham khảo quan trọng cho các mô hình dự đoán tỷ lệ sống sót (xem Bảng 1).
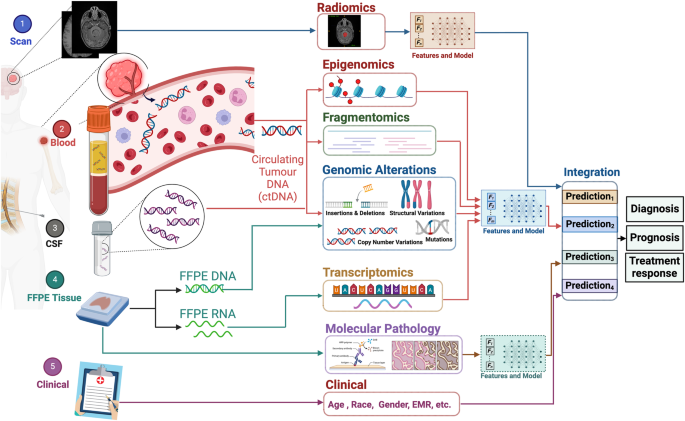
Ngoài các loại dữ liệu được sử dụng tiêu chuẩn hơn, các phương pháp sáng tạo như sinh thiết lỏng đã xuất hiện để phát hiện sớm các khối u não35. Phân tích DNA khối u tuần hoàn (ctDNA), một phương pháp không xâm lấn, theo dõi đột biến khối u và thay đổi di truyền thông qua các đoạn DNA khối u trong máu36,37. Việc tích hợp các loại dữ liệu đa dạng và công nghệ tiên tiến này cho phép một kỷ nguyên mới của các phương pháp tiếp cận chính xác, xâm lấn tối thiểu và hiệu quả để chẩn đoán và điều trị khối u não, khắc phục những hạn chế của các phương pháp chẩn đoán thông thường. Việc tích hợp nhiều nguồn dữ liệu thông qua hợp nhất dữ liệu đa phương thức giúp tăng cường độ chính xác của các phân tích bằng cách cung cấp cái nhìn toàn diện hơn về đặc điểm và hành vi của khối u38(Hình. 2). Tổng quan ngắn gọn về từng loại dữ liệu, bao gồm mô tả và mục đích của nó, được cung cấp trong Bảng 1.
Hiển thị là khung cấu trúc của một phương pháp tích hợp đa phương thức được thiết kế để cải thiện quản lý khối u não. Quá trình này liên quan đến việc đồng hóa dữ liệu từ năm nguồn khác nhau, mỗi nguồn đóng góp thông tin duy nhất. Từ quét MRI, dữ liệu phóng xạ được tạo ra. Dữ liệu này bao gồm các hình ảnh MRI được phân đoạn đạt được thông qua các kỹ thuật phân đoạn do AI điều khiển, cung cấp thông tin về các đặc điểm không gian của khối u. Các mẫu máu mang lại ctDNA, cho phép trích xuất các thay đổi biểu sinh, phân mảnh và bộ gen thông báo cho cảnh quan phân tử của khối u. Các mẫu CFS cung cấp DNA không có tế bào (cfDNA), cung cấp thông tin thay đổi bộ gen và góp phần hiểu biết toàn diện về hồ sơ di truyền của khối u. Các mẫu mô nhúng parafin (FFPE) cố định chính thức cung cấp dữ liệu bệnh lý phiên mã và phân tử, cung cấp thông tin về biểu hiện gen và cấu trúc tế bào. Thông tin lâm sàng như tuổi, chủng tộc, giới tính và dữ liệu hồ sơ y tế điện tử (EMR) bổ sung cho dữ liệu phân tử và hình ảnh, làm phong phú thêm hồ sơ của bệnh nhân. Đối với mỗi phương thức này, việc trích xuất tính năng được thực hiện, tạo ra một tập hợp các đặc điểm thông tin. Sau đó, các mô hình dự đoán được áp dụng cho từng bộ dữ liệu để ước tính các kết quả chính liên quan đến chẩn đoán, tiên lượng và đáp ứng điều trị. Trong quá trình tích hợp đa phương thức muộn, các dự đoán từ các mô hình riêng biệt này được hợp nhất để cải thiện hiệu suất và độ chính xác. Bằng cách tổng hợp thông tin từ nhiều nguồn và phương thức khác nhau, phương pháp tích hợp giúp tăng cường độ tin cậy và độ chính xác của chẩn đoán ung thư thần kinh, tiên lượng và dự đoán đáp ứng điều trị (Được tạo bằng BioRender.com).
Ngoài các bộ dữ liệu thể chế, nhiều bộ dữ liệu công khai đóng một vai trò quan trọng trong việc đánh giá các thuật toán dựa trên AI để chẩn đoán, tiên lượng và lập kế hoạch điều trị khối u não. Phù hợp với nhu cầu nghiên cứu đa dạng, các bộ dữ liệu này bao gồm các khía cạnh khác nhau của bệnh. Lưu trữ hình ảnh ung thư (TCIA) đáng chú ý trong số các bộ dữ liệu khối u não nói chung, cung cấp một kho lưu trữ toàn diện dữ liệu hình ảnh y tế, bao gồm quét MRI, CT và PET cho các loại khối u khác nhau39. MICCAI BraTS Challenge cung cấp các bộ dữ liệu phân đoạn khối u não được tiêu chuẩn hóa hàng năm, lý tưởng để đánh giá các thuật toán tập trung vào phân định khối u chính xác40.
Đối với các loại khối u cụ thể, các tài nguyên như bộ dữ liệu NCI TARGET bao gồm các phần dành riêng cho u nguyên bào thần kinh đệm (TCGA-GBM) và u thần kinh đệm cấp thấp hơn (TCGA-LGG)41. Các nền tảng bổ sung như liên minh dữ liệu mở và chung dữ liệu NCI cung cấp các bộ dữ liệu truy cập mở trên các lĩnh vực khoa học, bao gồm các bộ dữ liệu y tế và khối u não42,43. Việc lựa chọn bộ dữ liệu phù hợp nhất phụ thuộc vào các yếu tố như loại khối u, phương thức hình ảnh, loại dữ liệu (MRI, CT, PET, v.v.), tính khả dụng của chú thích sự thật cơ bản và kích thước dữ liệu, cho phép các nhà nghiên cứu điều chỉnh lựa chọn của họ với các lợi ích nghiên cứu cụ thể cho các cuộc điều tra dựa trên AI về chẩn đoán khối u não và lập kế hoạch điều trị.
Những tiến bộ trong tiền xử lý tăng cường AI để phân tích khối u não chính xác
Trong phân tích khối u não, AI đã giải quyết những thách thức trong việc điều hướng giải phẫu não và sự biến đổi khối u và tăng cường đáng kể các bước tiền xử lý quan trọng để chẩn đoán, tiên lượng và lập kế hoạch điều trị chính xác. Giải quyết các vấn đề về tính nhất quán không gian, các thuật toán được hỗ trợ bởi AI, chẳng hạn như các thuật toán được tích hợp vào trình xem BrainNet, sửa các tạo tác và biến dạng trong hình ảnh MRI44. Sự điều chỉnh này tạo điều kiện cho việc định vị và phân đoạn khối u chính xác hơn, điều này rất quan trọng để phân tích khối u não hiệu quả.
Hơn nữa, AI hợp lý hóa quá trình nội địa hóa khối u phức tạp với độ chính xác vượt trội, như được chứng minh bằng các thuật toán được đánh giá trên bộ dữ liệu BraTS40. Đáng chú ý, một số phương pháp được hỗ trợ bởi AI đã đạt được độ chính xác cao trong việc khoanh vùng các khối u, do đó nâng cao hiệu quả cho các bác sĩ X quang và giảm khả năng xảy ra lỗi của con người45,46. Phân đoạn hình ảnh thông qua CNN, vốn rất giỏi trong việc khám phá các mẫu phức tạp từ dữ liệu, đã nổi lên như một công cụ mạnh mẽ47,48,49,50,51. Các thuật toán do AI điều khiển, bao gồm thuật toán nnU-Net52, thể hiện sự thành thạo đặc biệt trong việc tự động hóa nhiệm vụ quan trọng là phân đoạn các mô bình thường trong hình ảnh y tế. Phân đoạn này rất quan trọng để phân tích khối u, hỗ trợ các bác sĩ X quang xác định các khu vực cần tránh trong quá trình xạ trị hoặc phẫu thuật52. Trong những phát triển gần đây, khung học tập liên kết đã chứng minh kết quả tương đương hoặc vượt trội trong việc phân đoạn tự động các khối u trẻ em hiếm gặp từ hình ảnh MRI. Cách tiếp cận này thúc đẩy dữ liệu từ các tổ chức đa dạng trong khi vẫn đảm bảo tính bảo mật tối đa của thông tin bệnh nhân24.
Việc tích hợp dữ liệu đa phương thức giúp nâng cao hiệu quả phát hiện bằng cách khai thác các nguồn thông tin đa dạng53. Cảnh quan của DL giới thiệu các kiến trúc sáng tạo, với một số ví dụ đáng chú ý, bao gồm cả U-Net 3D46, DeepMedic54và V-Net55. 3D U-Net, được thiết kế để vượt trội trong việc phân đoạn hình ảnh 3D của u nguyên bào thần kinh đệm và được công nhận về đào tạo đơn giản và hiệu quả nhất quán, đạt được kết quả đáng chú ý trong phân đoạn khối u não. DeepMedic54, được biết đến với sự mạnh mẽ trong việc quản lý tiếng ồn và hiện vật, là đối thủ cạnh tranh mạnh mẽ với U-Net 3D, được đào tạo về hình ảnh u thần kinh đệm. V-Net, một sự đổi mới non trẻ được thiết kế để phân đoạn chính xác hình ảnh y tế thể tích, thiết lập sức mạnh của nó trong việc phân đoạn cả hình ảnh MRI 2D và 3D55. Nhìn chung, vai trò của AI trong các bước tiền xử lý này cho phép các bác sĩ X quang tiến hành phân tích khối u não với độ chính xác và hiệu quả cao.
AI trong chẩn đoán khối u não
Chẩn đoán khối u não liên quan đến việc xác định và mô tả đặc điểm của sự tăng trưởng hoặc khối lượng bất thường trong não, sử dụng các phương pháp hình ảnh y tế, bệnh lý và lâm sàng khác nhau để xác định bản chất, vị trí và đặc điểm của khối u55. Các khối u não khác nhau dựa trên nguồn gốc, vị trí, mô học, bệnh ác tính và tuổi của bệnh nhân, và phân loại chúng là rất quan trọng để chẩn đoán, tiên lượng và lập kế hoạch điều trị55. Những khối u này bao gồm các phân nhóm đa dạng, mỗi loại được đặc trưng bởi nguồn gốc tế bào và đặc điểm mô học riêng biệt. Trong khi u thần kinh đệm và MB loại thấp và cao cấp ở trẻ em thường gặp nhất ở trẻ em, u nguyên bào thần kinh đệm, u thần kinh đệm lan tỏa và u màng não chiếm ưu thế ở người lớn56. Do tầm quan trọng của chúng, trọng tâm chủ yếu của nghiên cứu là u nguyên bào thần kinh đệm và u thần kinh đệm lan tỏa khác ở người lớn và MB, và u thần kinh đệm cấp thấp và cao cấp ở trẻ em57,58. Xác định chính xác phân nhóm khối u cho phép các bác sĩ lâm sàng tùy chỉnh các phương pháp chẩn đoán, dự đoán hành vi bệnh và thông báo các liệu pháp nhắm mục tiêu59. Chữ ký di truyền và mô học độc đáo liên quan đến các loại khối u khác nhau cung cấp thông tin về tính tích cực và đáp ứng điều trị, hướng dẫn lựa chọn phương thức hình ảnh, đánh giá dấu ấn sinh học và kế hoạch điều trị60.
Các khối u não thường được xác định trên CT được thực hiện trong môi trường phòng cấp cứu, trước khi được đặc trưng thêm thông qua MRI và được chẩn đoán dứt khoát thông qua kiểm tra mô bệnh học56. Tiêu chuẩn chăm sóc trong bệnh học thần kinh hiện nay bao gồm xét nghiệm phân tử và di truyền cho nhiều loại khối u, được hướng dẫn bởi các phát hiện mô học ban đầu57. Các phương pháp chẩn đoán hiện tại phải đối mặt với những thách thức58,59,60 chẳng hạn như phát hiện sớm do che giấu khối u61, giới hạn hình ảnh20, và các vấn đề về hình dung các khối u nhỏ hoặc sâu62,63, khó khăn trong việc phân biệt các loại khối u64, thủ thuật xâm lấn với các rủi ro liên quan65, và sự không đồng nhất của khối u não66. Những cách tiếp cận này bị cản trở bởi các quy trình tốn thời gian, khả năng tiếp cận hạn chế và sự thay đổi giải thích giữa các chuyên gia, làm nổi bật sự cần thiết của các phương pháp dựa trên AI tiên tiến16,67.
AI có thể gia tăng giá trị ở tất cả các bước chẩn đoán khối u, với phần lớn các nghiên cứu hiện tại cố gắng tạo ra các mô hình dự đoán được đào tạo bằng cách sử dụng dữ liệu hình ảnh, dữ liệu bệnh lý hoặc cả hai chế độ dữ liệu kết hợp68. Việc tích hợp các mô hình AI trong chẩn đoán khối u não cho thấy tiềm năng, đặc biệt là trong việc phân biệt giữa u thần kinh đệm và di căn não đơn độc bằng các phương pháp phân tích hình ảnh định lượng69,70. Hình ảnh thần kinh cung cấp một cái nhìn độc đáo về toàn bộ khối u không thay đổi, trong khi các phân tích bệnh lý cung cấp một cái nhìn sâu hơn về các đặc điểm tế bào và phân tử của khối u. ML, như một yếu tố quan trọng của AI, đang góp phần vào những tiến bộ trong chẩn đoán khối u não bằng cách tăng cường độ chính xác, đẩy nhanh phân tích hình ảnh, cho phép phát hiện sớm và cải thiện sự khác biệt giữa các loại khối u. Tiến bộ gần đây trong CV, ML và DL có tiềm năng giải quyết các thách thức và cải thiện chăm sóc bệnh nhân trong chẩn đoán khối u não45.
X quang được hỗ trợ bởi AI và các phương pháp chẩn đoán dựa trên mô học
Chẩn đoán khối u não dựa trên X quang và mô học liên quan đến việc trích xuất các đặc điểm định lượng từ hình ảnh y tế như quét MRI hoặc H &E WHI để nắm bắt hình thái, kết cấu và mối quan hệ không gian của khối u. Các phương pháp trích xuất tính năng truyền thống như phân tích kết cấu (Ma trận đồng xuất hiện cấp độ xám (GLCM), Ma trận độ dài chạy cấp độ xám (GLRLM) và Haralick71,72), Phân tích hình dạng73, Phân tích cường độ74, Phân tích dựa trên Wavelet75, được bổ sung bởi các cách tiếp cận mới hơn. Sau đó, ML và DL xây dựng các mô hình dự đoán, cho phép cách tiếp cận chẩn đoán dựa trên dữ liệu, được cá nhân hóa31,76,77. Các kỹ thuật phổ biến bao gồm CNN, RNN, máy biến áp tầm nhìn, mạng đối nghịch sinh sản (GAN)78, hỗ trợ máy vector và rừng ngẫu nhiên77 (Bảng bổ sung 1). Các mô hình được tạo ra từ nhiều chuỗi, chẳng hạn như mpMRI đã được chứng minh là chính xác hơn khi so sánh với các mô hình trình tự đơn79 để phát hiện khối u, đánh giá cấp độ và hướng dẫn lập kế hoạch điều trị80.
Các phương pháp chẩn đoán dựa trên mô học, được liên kết bởi cuốn sách phân loại CNS năm 2021 của WHO (Tổ chức Y tế Thế giới), là trung tâm của bệnh lý khối u não. Phân tích dựa trên mô học bao gồm các kỹ thuật phân tử khác nhau tận dụng dữ liệu mô học để tăng cường chẩn đoán khối u não. Methylome profiling, một kỹ thuật có ảnh hưởng gần đây sử dụng phân loại dựa trên AI / ML, đã trở thành một kỹ thuật có ảnh hưởng để phân loại và chẩn đoán khối u não81. Mặc dù phân loại năm 2021 của WHO hỗ trợ việc sử dụng các bộ phân loại methylome cho các khối u não khác nhau như là tiêu chí thiết yếu hoặc mong muốn, nhưng vẫn có cuộc tranh luận đang diễn ra về phương pháp tốt nhất và khả năng tiếp cận hạn chế của các xét nghiệm chẩn đoán34. U thần kinh đệm sâu82, một hệ thống sàng lọc chẩn đoán dựa trên AI, cung cấp kết quả nhanh chóng (<90 giây) bằng cách hợp lý hóa chẩn đoán phân tử GMG bằng cách sử dụng hình ảnh mô học Raman (SRH) được kích thích. Hệ thống sáng tạo này đã được phát triển và xác nhận trên một đoàn hệ đa trung tâm, làm nổi bật tiềm năng của nó để chẩn đoán khối u não nhanh chóng và chính xác82.
Hơn nữa, các phương pháp tiếp cận sáng tạo sử dụng phóng xạ trên quét tưới máu MRI đã chứng minh khả năng dự đoán đột biến IDH, cung cấp thông tin có giá trị cho chẩn đoán và lập kế hoạch điều trị83. Quang phổ Terahertz đã được khám phá như một kỹ thuật không xâm lấn để dự đoán đột biến IDH trong các mẫu mô u thần kinh đệm, trình bày một giải pháp thay thế đầy hứa hẹn cho các phương pháp hiện có84. Hơn nữa, các kỹ thuật phân tích tiên tiến được áp dụng cho quét PET / CT 18F-FET đã cho phép dự đoán cả cấp độ u thần kinh đệm và tình trạng đột biến IDH ở những bệnh nhân không được điều trị85. Đáng chú ý, một chữ ký hình ảnh học sâu (DLIS) đã được phát triển, đưa ra dự đoán chính xác về sự đồng xóa 1p / 19q trong u thần kinh đệm mức độ thấp lan tỏa thông qua quét MRI trước phẫu thuật, đưa ra một giải pháp thay thế không xâm lấn với tiềm năng chẩn đoán đáng kể86.
Sự tích hợp của hóa mô miễn dịch, hồ sơ methyl hóa, vi mảng nhiễm sắc thể, scRNA-seq87và NGS, với phân tích dựa trên mô học có thể tăng cường hơn nữa chẩn đoán khối u não81,88. Trong khi các phương pháp tiếp cận thông thường, sử dụng hình ảnh, sinh thiết mô và xét nghiệm di truyền, tự tin xác định nhiều khối u não bằng cách kết hợp mô học với những thay đổi di truyền cụ thể, vẫn tồn tại các trường hợp ngoại lệ, chẳng hạn như u sao bào cao cấp với các đặc điểm piloid, được giới thiệu trong phân loại năm 2021 của WHO88,89. Tình trạng đặc biệt này đòi hỏi hồ sơ methylome để chẩn đoán89, nhưng sự hiếm gặp của nó cho thấy rằng phân loại methylome phù hợp nhất cho các trường hợp cụ thể với các biểu hiện lâm sàng và bệnh lý không điển hình. Một phương pháp học sâu gần đây có tên là “Cá tầm”, có thể phân loại nhanh chóng và chính xác các loại khối u thần kinh trung ương trong quá trình phẫu thuật bằng cách sử dụng dữ liệu mảng methyl hóa thưa thớt thu được từ trình tự nanopore được tạo ra trong quá trình phẫu thuật. Nó phân loại các khối u thần kinh trung ương trong vòng 40 phút sau khi bắt đầu giải trình tự, với độ chính xác 72% trong cài đặt phẫu thuật thời gian thực90. Phương pháp này cho phép các bác sĩ phẫu thuật đưa ra quyết định sáng suốt hơn về mức độ cắt bỏ, có khả năng làm giảm nguy cơ biến chứng và cải thiện kết quả của bệnh nhân.
AI trong tiên lượng khối u não
Tiên lượng trong ung thư thần kinh liên quan đến việc ước tính tiến triển bệnh cho một cá nhân, xem xét kế hoạch điều trị, giai đoạn bệnh và vị trí91. Các chỉ số chính là tỷ lệ sống sót tổng thể (HĐH) và tỷ lệ sống không tiến triển (PFS), rất quan trọng để đánh giá tiên lượng và hướng dẫn điều trị92. Tuy nhiên, các phương pháp thông thường dựa vào giai đoạn bệnh và các biến lâm sàng phải đối mặt với những hạn chế, bao gồm sự phức tạp về diễn giải, thành kiến và sự cần thiết của các bộ dữ liệu mở rộng. Đạt được độ chính xác cho chăm sóc cá nhân trong việc dự đoán tái phát và tỷ lệ sống sót vẫn còn thách thức với các phương pháp thông thường.
Trong chăm sóc khối u não, AI đóng một vai trò quan trọng trong việc thúc đẩy khả năng tiên lượng. Các kỹ thuật ML và DL đang ngày càng được khai thác để dự đoán hệ điều hành và PFS, tận dụng các tính năng được trích xuất từ dữ liệu hình ảnh trước khi xử lý. Các nghiên cứu đáng chú ý, bao gồm chữ ký phóng xạ từ quét T1 và FLAIR MRI của bệnh nhân u nguyên bào thần kinh đệm69và quét T1, T2 và FLAIR từ những bệnh nhân chưa điều trị, cho thấy hứa hẹn đáng kể trong việc dự đoán PFS và HĐH93,94. Các mô hình AI hoạt động tốt hơn các biến lâm sàng thông thường và chứng minh sự xuất sắc khi kết hợp với các thuộc tính lâm sàng ở bệnh nhân u nguyên bào thần kinh đệm95,96. Đáng chú ý, các mô hình dựa trên MRI trọng số T297 và các đặc điểm phóng xạ từ phù quanh khối u cho thấy mối liên quan với kết quả sống sót, vị trí tái phát và phân nhóm phân tử98, đặc biệt là trong u thần kinh đệm97và bệnh nhân u nguyên bào thần kinh đệm99. Các mô hình dựa trên DL được tạo ra để xác định các khối u và dự báo vị trí tái phát, đôi khi trước khi các bác sĩ X quang có thể phát hiện ra nó100. Những mô hình này, sử dụng các phương pháp hình ảnh khác nhau, làm nổi bật khả năng dự đoán đặc biệt của AI97,99 (Bảng 2).
Hơn nữa, sự không đồng nhất trong khối u và độ dẻo của trạng thái tế bào đã được xác định là động lực chính cho tình trạng kháng trị liệu của u nguyên bào thần kinh đệm30. Hồ sơ phiên mã không gian và tiên lượng từ hình ảnh mô học đã được dự đoán bằng cách sử dụng khung DL này, làm sáng tỏ tiềm năng của AI trong việc làm sáng tỏ các khía cạnh phức tạp của hành vi khối u30. Ngoài ra, việc xác định đột biến IDH đã được tận dụng để hướng dẫn tiên lượng, trong khi định nghĩa về u nguyên bào thần kinh đệm đã được tinh chỉnh thông qua phân tích chất xúc tiến TERT, khuếch đại EGFR, tăng nhiễm sắc thể 7 và mất nhiễm sắc thể 10. Ngoài ra, H3F3A đã nổi lên như một dấu hiệu quan trọng cho các khối u trẻ em xâm lấn101.
AI trong quản lý điều trị khối u não
Ngoài việc tăng thêm giá trị cho cả khả năng chẩn đoán và tiên lượng, AI đã được sử dụng để cải thiện kế hoạch điều trị khối u não và đánh giá đáp ứng điều trị102. Nó biến đổi các phương pháp điều trị và tăng cường độ chính xác bằng cách hỗ trợ xác định và mô tả đặc điểm của các khối u não. Nó hướng dẫn các bác sĩ lâm sàng trong việc xác định các chiến lược điều trị phù hợp nhất cho từng bệnh nhân. Quá trình nhiều mặt này bao gồm các kỹ thuật đa dạng, bao gồm hình ảnh, đánh giá lâm sàng, sinh thiết và phân tích phân tử, để xác định chính xác sự hiện diện, loại, vị trí và mức độ của khối u.
Các phương pháp dựa trên AI vượt trội trong việc dự đoán đáp ứng trị liệu, cho phép cải thiện kế hoạch điều trị trên các bệnh ung thư khác nhau103. Các phương pháp tiếp cận mới, chẳng hạn như dự đoán phản ứng với xạ phẫu bằng dao gamma đối với các khối u não di căn bằng cách sử dụng các tính năng phóng xạ104 từ quét T1 và FLASH tăng cường độ tương phản và sử dụng các mô hình dự đoán dựa trên bản đồ ADC tiền điều trị để dự báo đáp ứng với xạ trị, cho thấy hiệu quả của AI104. Các mô hình tích hợp, kết hợp phóng xạ với các thuộc tính lâm sàng, đánh giá hiệu quả đáp ứng xạ trị cho bệnh nhân di căn não do ung thư vú và ung thư phổi nguyên phát trên các nhóm bệnh nhân đa trung tâm105. Phân tích không đồng nhất không gian của phù quanh khối u (ED) trong u nguyên bào thần kinh đệm hỗ trợ xác định môi trường sống có nguy cơ cao trong ED, dẫn đến tăng cường lập kế hoạch điều trị106. Trong khi việc xác định dấu hiệu quan trọng MGMT cho tình trạng kháng temozolomide (TMZ) ở bệnh nhân u nguyên bào thần kinh đệm đưa ra những thách thức, các phương pháp phóng xạ dựa trên AI nổi lên như là yếu tố dự đoán về cả tình trạng MGMT và phản ứng TMZ, cung cấp những hiểu biết có giá trị cho các quyết định điều trị sáng suốt101.107 (Bảng 3).
Phân tích tích hợp đa phương thức và đa quy mô
Trong các phương pháp tiếp cận đa phương thức và đa quy mô, hy vọng là sự hiểu biết toàn diện hơn về các khối u não thông qua việc tích hợp bộ gen, bệnh lý và dữ liệu phóng xạ. Bộ gen, đặc biệt là thông qua các kỹ thuật như NGS, đóng một vai trò nổi bật trong việc làm sáng tỏ cảnh quan di truyền của các khối u não, cung cấp thông tin về sự thay đổi bộ gen của chúng88. Phân nhóm phân tử và dấu ấn sinh học được xác định đóng một vai trò quan trọng trong y học chính xác cá nhân hóa, tác động đến việc phát hiện sớm, tiên lượng và dự đoán đáp ứng điều trị. Cách tiếp cận tích hợp này, khi kết hợp với dữ liệu lâm sàng, nâng cao sự hiểu biết của chúng tôi và đặt nền tảng cho các phương pháp điều trị phù hợp nhắm vào các thay đổi di truyền cụ thể.
Bổ sung cho nền tảng gen này, các kỹ thuật hình ảnh đa phương thức như MRI, CT và PET đóng góp một lớp phong phú cho tấm thảm tích hợp, mặc dù có những thách thức về chi phí và thời gian108. Khi kết hợp với chuyên môn lâm sàng và các dữ liệu chẩn đoán khác, hình ảnh đa mô thức giúp tăng cường đáng kể độ chính xác chẩn đoán. Sự tích hợp của bộ gen và phóng xạ, được tạo điều kiện bởi AI, nổi lên như một lực lượng cách mạng trong việc hiểu và điều trị các khối u não.
Hơn nữa, những tiến bộ của AI vượt ra ngoài các dự đoán đơn phương, mở ra một kỷ nguyên của các phương pháp tiên lượng và điều trị đa phương thức. Các phương pháp tiếp cận đa phương thức, đa phương thức này trích xuất các tính năng từ các nguồn dữ liệu đa dạng, bao gồm hình ảnh phóng xạ và hình ảnh đa phương thức, dẫn đến sự hiểu biết toàn diện và chính xác hơn về quỹ đạo bệnh100 (Hình. 2).
Những thách thức và hạn chế của AI trong chẩn đoán, tiên lượng và điều trị khối u não
Mặc dù tích hợp thành công các mô hình AI trong các bước khác nhau của quản lý khối u não, những thách thức vẫn tồn tại. Những thách thức này bao gồm quyền truy cập hạn chế vào dữ liệu chất lượng cao, mối quan tâm về khả năng diễn giải và khả năng giải thích của các mô hình DL và nhu cầu khái quát hóa trên các quần thể và loại khối u khác nhau109. Khả năng tái tạo của các đặc điểm dựa trên phóng xạ trên các viện khác nhau phải đối mặt với những thách thức do sự thay đổi trong các thông số thu nhận hình ảnh, bao gồm máy móc, mô hình và lượng tương phản110. Đặc biệt, việc đạt được khả năng tái tạo phức tạp hơn trong bức xạ MR so với bức xạ CT111. Để chuẩn hóa phóng xạ, việc giới thiệu điểm chất lượng phóng xạ (RQS) là rất quan trọng112. Tuy nhiên, bất chấp tầm quan trọng của việc xác nhận phương pháp AI trong ung thư thần kinh bằng cách sử dụng bộ dữ liệu bên ngoài, chỉ có 29,4% nghiên cứu ban đầu bao gồm xác nhận bên ngoài113.
Ngoài ra, trong quản lý khối u não, rõ ràng là sự chênh lệch chủng tộc tạo ra các động lực phức tạp được định hình bởi chủng tộc, các biến số kinh tế xã hội và ảnh hưởng địa lý114. Sự phức tạp này mở rộng đến nhiều khía cạnh khác nhau, bao gồm các khuyến nghị cho phẫu thuật khối u não115, nhấn mạnh tầm quan trọng của việc giải quyết sự chênh lệch như vậy trong các phương pháp dựa trên AI trong toàn bộ phổ quản lý khối u não để thúc đẩy chăm sóc ung thư. Hơn nữa, sự chênh lệch về tỷ lệ và kết quả khối u não, đặc biệt là trong u nguyên bào thần kinh đệm, biểu hiện khác nhau giữa nam và nữ116. Điều này nhấn mạnh sự cần thiết của các phương pháp tiếp cận dựa trên AI đối với các yếu tố ảnh hưởng liên quan đến giới tính về tỷ lệ mắc, tỷ lệ sống, sinh học khối u, di truyền, đáp ứng điều trị và tiên lượng. Ưu điểm chính của các mô hình này nằm ở việc đưa ra các dự đoán nâng cao để điều trị cá nhân hóa và tiềm năng phát hiện sớm bằng cách tính đến các đặc điểm giới tính cụ thể.
Ý nghĩa đạo đức, pháp lý và xã hội của AI trong quản lý khối u não
Việc tích hợp AI trong chẩn đoán, tiên lượng và điều trị khối u não làm tăng các cân nhắc quan trọng về đạo đức, pháp lý và xã hội117. Các mối quan tâm đạo đức chính bao gồm đảm bảo quyền riêng tư của bệnh nhân thông qua các biện pháp bảo mật dữ liệu mạnh mẽ, có được sự đồng ý có hiểu biết, giải quyết sự công bằng thuật toán và thúc đẩy tính minh bạch trong các thuật toán AI và trách nhiệm giải trình để xây dựng và duy trì niềm tin của bệnh nhân28. Những đổi mới như học tập liên kết nhằm giải quyết thách thức về quyền riêng tư trong AI bằng cách cho phép đào tạo mô hình hợp tác giữa nhiều bên mà không cần chia sẻ dữ liệu thô24. Các mệnh lệnh đạo đức mở rộng để giải quyết các thành kiến và đảm bảo tiếp cận công bằng. Các cân nhắc pháp lý, bao gồm trách nhiệm pháp lý đối với các lỗi do AI tạo ra, các tiêu chuẩn sơ suất y tế và tuân thủ quy định, nhấn mạnh sự cần thiết phải có các khung pháp lý mạnh mẽ. Các nỗ lực hợp tác liên quan đến các nhà hoạch định chính sách, cơ quan quản lý và chuyên gia pháp lý là rất quan trọng để làm rõ trách nhiệm, bảo vệ sự an toàn của bệnh nhân và thúc đẩy phát triển AI có trách nhiệm. Ý nghĩa xã hội, chẳng hạn như tác động đến mối quan hệ giữa bệnh nhân và bác sĩ, trao quyền cho bệnh nhân và chênh lệch về chăm sóc sức khỏe, đòi hỏi phải xem xét cẩn thận. AI có tiềm năng trao quyền cho bệnh nhân bằng cách cung cấp thông tin được cá nhân hóa và cho phép ra quyết định chung117.118. Tuy nhiên, khả năng tiếp cận công bằng và khả năng chi trả của chăm sóc sức khỏe do AI điều khiển cần được giải quyết để tránh làm trầm trọng thêm sự chênh lệch hiện có117.118.
Sự thảo luận
Đánh giá này nhấn mạnh tác động biến đổi của AI trong quản lý khối u não, biểu thị sự thay đổi mô hình trong chăm sóc sức khỏe nhằm giải quyết những thách thức lâu dài. Sự thành thạo của AI trong các kỹ thuật ML và DL, đặc biệt là trong phân đoạn hình ảnh, tính nhất quán không gian và dự đoán, giúp tăng cường độ chính xác trong việc xác định và mô tả các khối u não. Độ chính xác này góp phần cải thiện chẩn đoán, tiên lượng và lập kế hoạch điều trị cá nhân hóa. Sự tích hợp liền mạch của các loại dữ liệu đa dạng, từ hình ảnh y tế đến bộ gen, cùng với lịch sử lâm sàng, cho phép hiểu toàn diện về đặc điểm khối u, định hình tiên lượng và kế hoạch điều trị cá nhân hóa. Tiềm năng của AI trong việc trao quyền cho các bác sĩ lâm sàng theo dõi thời gian thực, lập kế hoạch điều trị nâng cao và tối ưu hóa được nhấn mạnh, hứa hẹn cải thiện kết quả của bệnh nhân.
Khả năng tiên lượng của các mô hình dựa trên AI vượt qua các biến lâm sàng thông thường, cung cấp độ chính xác dự đoán vượt trội và tinh chỉnh dự đoán tỷ lệ sống sót30. Việc tích hợp AI trong việc dự đoán đáp ứng điều trị, thời gian sống sót và vị trí tái phát là một tiến bộ đáng kể, cho phép các liệu pháp chính xác, được cá nhân hóa phù hợp với đặc điểm khối u riêng lẻ và dữ liệu cụ thể của bệnh nhân. Chẩn đoán dựa trên AI không chỉ tạo điều kiện theo dõi thời gian thực mà còn cải thiện việc lập kế hoạch và tối ưu hóa điều trị. Phần này nhấn mạnh tiềm năng của AI trong việc cung cấp các can thiệp chính xác, cá nhân hóa và hiệu quả hơn, góp phần nâng cao kết quả của bệnh nhân. Các hệ thống hỗ trợ quyết định lâm sàng, được trao quyền bởi AI, không chỉ cung cấp các khuyến nghị điều trị dựa trên bằng chứng mà còn đóng góp vào nghiên cứu đang diễn ra bằng cách tạo ra những hiểu biết và dấu ấn sinh học mới.
Những cân nhắc về đạo đức trong việc tích hợp AI trong chẩn đoán, tiên lượng và điều trị khối u não được thừa nhận, bao gồm quyền riêng tư dữ liệu, công bằng thuật toán, trách nhiệm pháp lý và ý nghĩa xã hội. Các khung pháp lý mạnh mẽ và các nỗ lực hợp tác như học tập liên kết được coi là cần thiết để giải quyết những thách thức này đối với sự phát triển AI có trách nhiệm và sự chấp nhận của xã hội trong chăm sóc sức khỏe. Bất chấp những thách thức như chi phí thu thập dữ liệu và sự phức tạp trong diễn giải, tích hợp AI hứa hẹn đáng kể, mang lại triển vọng chăm sóc bệnh nhân chính xác và được cá nhân hóa trong tương lai. Tuy nhiên, thay đổi lực lượng lao động và đào tạo có thể cần thiết để tích hợp hiệu quả các công nghệ AI vào các cơ sở chăm sóc sức khỏe. Sự chấp nhận đạo đức và xã hội của AI trong chăm sóc sức khỏe phụ thuộc vào giao tiếp minh bạch, giải quyết các mối quan tâm về quyền riêng tư và thúc đẩy các hoạt động công bằng và toàn diện.
Nhìn chung, AI mở rộng ảnh hưởng của nó vào việc lập kế hoạch điều trị, cách mạng hóa các chiến lược điều trị và góp phần đáng kể vào việc cải thiện kết quả của bệnh nhân. Việc tích hợp AI vào bối cảnh điều trị hứa hẹn cho các can thiệp được cá nhân hóa và hiệu quả trong ung thư thần kinh.
Một tầm nhìn cho tương lai: một loạt các phương pháp tiếp cận
Việc tích hợp AI trong chẩn đoán, điều trị và tiên lượng khối u não đã có những tiến bộ đáng kể, nhưng vẫn còn những khoảng trống và hướng đi đầy hứa hẹn trong tương lai để khám phá. Tích hợp dữ liệu đa phương thức108, các chiến lược theo dõi, chẩn đoán và điều trị thích ứng theo thời gian thực có tiềm năng nâng cao độ chính xác chẩn đoán và kết quả điều trị90. AI có thể đóng một vai trò quan trọng trong việc tiên lượng dài hạn và lập kế hoạch chăm sóc sống sót, hỗ trợ việc ra quyết định điều trị. Thu hẹp khoảng cách giữa thực hành lâm sàng và nghiên cứu thông qua các mạng chia sẻ dữ liệu có thể đẩy nhanh quá trình phát triển và xác nhận mô hình AI. Tính minh bạch và khả năng giải thích của các mô hình AI là điều cần thiết để đạt được sự tin tưởng và chấp nhận trong môi trường lâm sàng119.120. Các cân nhắc về đạo đức và các nguyên tắc thiết kế lấy con người làm trung tâm phải được ưu tiên để đảm bảo tích hợp AI có trách nhiệm và lấy bệnh nhân làm trung tâm. Bằng cách giải quyết các khía cạnh này, AI có tiềm năng cách mạng hóa việc chăm sóc khối u não và cải thiện kết quả của bệnh nhân120.
Hình dung tương lai của phân tích khối u não, DL đứng ở vị trí hàng đầu, nhưng các kỹ thuật khác nhau vẫy gọi khám phá dựa trên các ứng dụng cụ thể và tính sẵn có của dữ liệu. Cải thiện các phương pháp hình ảnh, chẳng hạn như chụp cộng hưởng từ chức năng (fMRI)121 và hình ảnh tensor khuếch tán (DTI)122, cung cấp đặc điểm khối u chính xác hơn, bất chấp những thách thức như nhạy cảm với tiếng ồn, chuyển động đầu, biến dạng từ trường và chi phí tính toán123.124. Những tiến bộ tính toán, đặc biệt là CNN và các mô hình dựa trên Transformer, tăng cường độ chính xác trong việc phát hiện và phân loại các khối u não125.126.127. Hợp nhất dữ liệu đa phương thức108, bao gồm chụp MRI, CT và PET38, cùng với việc chuyển giao học tập bằng cách sử dụng các mô hình được đào tạo trước từ các bộ dữ liệu hình ảnh rộng lớn, giải quyết thách thức của dữ liệu y tế được gắn nhãn hạn chế77 (Bảng bổ sung 1).
Các phương pháp dựa trên đồ thị thúc đẩy các mối quan hệ vùng não phức tạp128, với mạng nơ-ron đồ thị (GNN) và mạng tích chập dựa trên đồ thị (GCN) chiếu sáng con đường mô hình hóa kết nối não và phát hiện ra những bất thường liên quan đến khối u129. Radiomics và kỹ thuật tính năng trích xuất một loạt các tính năng định lượng từ hình ảnh y tế, với các thuật toán ML chiếu sáng các mẫu và mối tương quan. AI có thể giải thích (XAI), một khía cạnh quan trọng, đảm bảo tính minh bạch và khả năng diễn giải thuật toán, một nền tảng trong các ứng dụng y tế130.131. Những nỗ lực gần đây đã hướng tới việc tạo ra các mô hình AI với đầu ra có thể giải thích được, thúc đẩy sự hiểu biết của các bác sĩ lâm sàng về các quy trình ra quyết định và do đó nuôi dưỡng niềm tin vào việc phát hiện và phân loại khối u não tự động. Các kỹ thuật tăng cường và tổng hợp dữ liệu, bao gồm xoay hình ảnh, chia tỷ lệ, lật và sự khéo léo của GAN, củng cố tính mạnh mẽ của tập dữ liệu đào tạo78.127 . Ngoài ra, AutoML và các công cụ tối ưu hóa siêu tham số hợp lý hóa việc tối ưu hóa kiến trúc và siêu tham số trong các thuật toán phát hiện khối u não, đỉnh cao là các mô hình hiệu quả và chính xác hơn.
Các nền tảng và bộ dữ liệu cộng tác, chẳng hạn như học tập liên kết24.132 Các kho lưu trữ dữ liệu khối u não được chú thích tỉ mỉ, đẩy nhanh quá trình đào tạo, đánh giá và đổi mới thuật toán đồng thời xúc tác cho các nỗ lực đo điểm chuẩn. Lĩnh vực phát hiện thời gian thực, được thúc đẩy bởi những tiến bộ trong phần cứng như bộ xử lý đồ họa (GPU) và mảng cổng lập trình trường (FPGA), mở ra tiềm năng xử lý hình ảnh y tế theo thời gian thực90.133 . Các thuật toán thời gian thực như vậy hứa hẹn hợp lý hóa quy trình làm việc lâm sàng và nâng cao chăm sóc bệnh nhân. Việc sử dụng gần đây các Mô hình ngôn ngữ lớn (LLM) trong nghiên cứu thần kinh thể hiện khả năng đáng chú ý để phân tích các nguồn dữ liệu đa dạng, đóng góp đáng kể cho chẩn đoán sớm, hỗ trợ bệnh nhân và hỗ trợ lâm sàng. Những thách thức đáng chú ý, bao gồm các mối quan tâm liên quan đến quyền riêng tư và thành kiến dữ liệu, nhấn mạnh sự bắt buộc đối với các nỗ lực hợp tác để đảm bảo sự phát triển có trách nhiệm của LLM trong thần kinh học134 (Bảng bổ sung 1).
Kết luận
Chúng tôi đã khám phá các ứng dụng biến đổi của AI, bao gồm CV, ML và DL, trong việc quản lý các khối u não. AI cho thấy hứa hẹn đáng kể trong chẩn đoán, tiên lượng và lập kế hoạch điều trị bằng cách phát hiện và phân loại hiệu quả các khối u não từ hình ảnh y tế. Thông qua các phân tích phóng xạ, bệnh lý và bộ gen, AI góp phần mô tả chính xác đặc điểm khối u. Trong điều trị, AI đóng một vai trò quan trọng trong việc lập kế hoạch, tối ưu hóa và dự đoán phản hồi, hỗ trợ các đề xuất được cá nhân hóa và giám sát thời gian thực. Việc tích hợp các phương pháp tiếp cận dựa trên AI phù hợp với y học chính xác và chăm sóc lấy bệnh nhân làm trung tâm. Tuy nhiên, việc áp dụng AI trong quản lý khối u não đòi hỏi phải xem xét cẩn thận các tác động đạo đức, pháp lý và xã hội, giải quyết các mối quan tâm liên quan đến quyền riêng tư dữ liệu và chênh lệch chăm sóc sức khỏe.
Các định hướng trong tương lai bao gồm thu hẹp khoảng cách nghiên cứu, khám phá các mô hình LLM, tích hợp dữ liệu đa phương thức và thúc đẩy giám sát thời gian thực. Các mô hình AI được đào tạo trên các bộ dữ liệu đa dạng hứa hẹn sẽ dự đoán đáp ứng điều trị và cải thiện kết quả của bệnh nhân. Sự phát triển và tinh chỉnh liên tục là điều cần thiết để khám phá toàn bộ tiềm năng và thách thức trong quản lý lâm sàng các khối u não, định vị AI như một công cụ có giá trị trong nghiên cứu và thực hành.

Ý kiến bạn đọc (0)